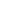美国尼古丁袋(口含烟)的监管政策分析
尼古丁袋在美国目前是受到美国食品药品监督管理局(FDA)的监管,其被当做是烟草产品,受到的监管要求主要包括购买年龄规定、标签和健康警告语、广告限制和上市前的申请授权(PMTA)。同时也会考虑多种因素,包括但不限于产品的所有组件、零件、成分和添加剂,以及用于制造成品的制造工艺等。
01FDA对于尼古丁袋(口含烟)的定义和分类
1.尼古丁袋(口含烟)的定义及要求:
根据FDA的定义,“尼古丁袋”是一种烟草产品。它们是一种小型纤维袋,与其他一些类型的口腔烟草制品不同,使用时不需要使用者吐痰。在使用过程中,这些小袋通常放置在牙龈和上唇之间,尼古丁在那里被人体吸收。尼古丁袋不用于加热或燃烧(燃烧)。
对于含有非烟草尼古丁(NTN)的尼古丁袋,从2022年4月14日起,还需要满足联邦法律H.R.2471的相关要求。该法律明确指出:FDA可以对任何来源含有尼古丁的烟草制品进行监管。
· 不分发这些产品的免费样品。
此外,从事NTN产品制造、制备、配制或加工的机构的所有者和经营者必须在 FDA 注册,并列出他们制造、制备、配制或加工用于商业分销的所有这些烟草产品。
同时,希望销售其含有NTN成分的产品制造商需要提交上市前申请(PMTA)并获得FDA授权,否则他们将受到FDA的执法; 目前对于已上市的NTN产品提交上市前申请(PMTA)的截止日期为2022年5月14日。
2.尼古丁袋(口含烟)的分类属性
FDA将现代尼古丁袋或口含烟归类为其它烟草产品(Other Tobacco Products),区别于无烟烟草产品(Smokeless Tobacco Products)。而传统的口含烟则类似于无烟烟草产品(Smokeless Tobacco Products)中的咀嚼烟草。
其它烟草产品(Other Tobacco Products)包含尼古丁袋(Nicotine Pouches)、尼古丁凝胶(Nicotine Gels)和可溶性的烟草产品(Dissolvable Tobacco Products)。

而无烟烟草产品(Smokeless Tobacco Products)则包括咀嚼烟草(Chewing tobacco)、干鼻烟(Dry snuff)、湿鼻烟(Moist snuff and snus)等。

02尼古丁袋(口含烟)的购买年龄、标签和警告语要求
1.首先是购买年龄。
《家庭吸烟预防和烟草控制法》规定限制向未成年人进行烟草营销和销售,这里的未成年人其实指的是未满21周岁的青少年。
2.其次是标签和警告语方面。
《家庭吸烟预防和烟草控制法》要求无烟烟草包装和广告应有更大、更明显的警告。无烟烟草包括湿鼻烟、咀嚼烟草和鼻烟等烟草制品。每个无烟烟草包装和广告都将包含以下警告标签声明之一:
l WARNING: This product can cause mouth cancer.
警告:本产品可能导致口腔癌。
l WARNING: This product can cause gum disease and tooth loss.
警告:本产品可能导致牙龈疾病和牙齿脱落。
l WARNING: This product is not a safe alternative to cigarettes.
警告:本产品不是香烟的安全替代品。
l WARNING: Smokeless tobacco is addictive.
警告:无烟烟草会上瘾。
对于无烟烟草包装,警告标签声明必须位于包装的两个主要面,并覆盖每面至少 30%。
对于广告,其警告标签声明必须至少覆盖广告面积的 20%。
· 烟草制品标签、包装和运输容器上的声明:“只允许在美国销售”。
传统口含烟属于无烟烟草产品,需要满足上述要求。
而对于现代尼古丁袋或口含烟来说,上述FD&C法案及其实施条例规定的包装和警告声明则不适用。但根据FDA对于尼古丁凝胶(属于其它烟草产品)销售的要求:其包装必须有警告语否则不能销售,所以还是建议在尼古丁袋或口含烟包装上增加警告语说明,符合同类产品的要求。比如:This product contains nicotine. Nicotine is an addictive chemical.
03尼古丁袋(口含烟)的PMTA申请简介
1.PMTA申请的内容
(9)对人群整体的影响(其中应包含对整体人群的健康影响评估)等。
2.尼古丁袋与电子烟相比在申报资料上的不同
由于电子烟和尼古丁袋在产品的构成及生产制造工艺上均存在不少的差距。电子烟其实是由两部分组成的,一部分是烟具,另一部分是烟油。两者需要结合在一起去进行申请,所以在申请资料的准备上,既需要烟具部分的资料还需要烟油部分的资料,包括烟油烟具的产品设计、生产制造、配方成分和健康风险评估等一系列配套资料。而尼古丁袋的构成更像烟油或者更准确的说是类似食品那样的产品,所以在申报方式上,更接近于食品的申报方式,提交的资料也是无论是生产工艺上、配方上、HPHCs,还是非临床毒理水平、临床药理学与行为学(BCP)等皆有不同。特别是毒理和临床方面的研究!
1)生产工艺上:提交配套的尼古丁袋生产工艺资料及文件,另外,还需要提供包装方面的工艺描述。但不需要提交像烟具这类的资料。
2)产品配方上:尼古丁袋需要像烟油那样提供配方、成分组成等资料,但也不需要烟具材料组成等内容。
3)HPHCs水平上:尼古丁袋主要通过经口吞咽的方式进食,并不会像电子烟那样经肺部吸入,因此,不需要分析烟气气溶胶部分的HPHCs水平,只需要分析类似烟油那样的HPHCs水平;另外,在HPHCs的项目种类上,也是不同于电子烟HPHCs的。
4)非临床毒理水平:尼古丁袋跟电子烟一样,均需要通过非临床方面的试验证明其毒性或健康危害水平要比市场上同类产品的更低,具有减害效果。电子烟可以跟传统烟(1R6F)或市场上在售的产品(比如VUSE,TJOY)比较。而尼古丁袋也需要这样,与尼古丁口香糖、鼻烟、香烟或其它无烟烟草产品等类似产品的数据比较来证明。
在非临床毒理水平申报资料上,比较充分的证明材料是包括HPHCs、体外细胞试验、体内动物实验等方面的数据。其中体外细胞试验可以是中性红吸收试验(NRU)、细菌回复突变(Ames)、体外微核试验(ivMN)等;体内动物实验可以是急性经口毒性试验、大鼠药代动力学研究或者小鼠18个月致癌性研究等等。
5)临床药理学与行为学(BCP):临床药理/行为学研究主要包括生物标志物(BOE)研究、不良反应的研究和个体行为学研究等。这些跟电子烟比较类似,目的均是证明尼古丁袋实际对健康影响的水平(比如上瘾性,致癌/致畸/致突变性,副作用等),同时也考察对非吸烟者的吸引力,是否会吸引未成年人和导致人群中的流行性?
G)与戒烟相比,改用这种产品的健康风险。
除了上述所说的不同方面,其它部分还包括尼古丁袋的稳定性研究情况、包装袋食品接触材料的迁移水平、文献研究情况综述、环境影响研究等等。
04FDA对尼古丁袋(口含烟)的申请审查和批准情况
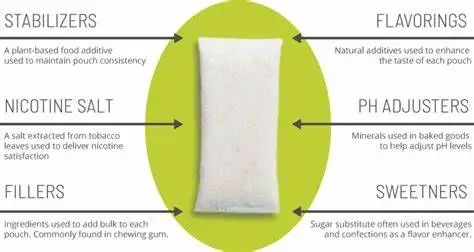
从2019年10月到2023年12月,FDA接收到按照“其它烟草产品”类别申请的PMTA总份数为2289份,其中获得受理(Accepted)的产品数有644份,被拒绝受理(Refuse to accept)的产品数有321份。而按照“其它烟草产品”类别申请的产品大部分都是尼古丁袋或口含烟。
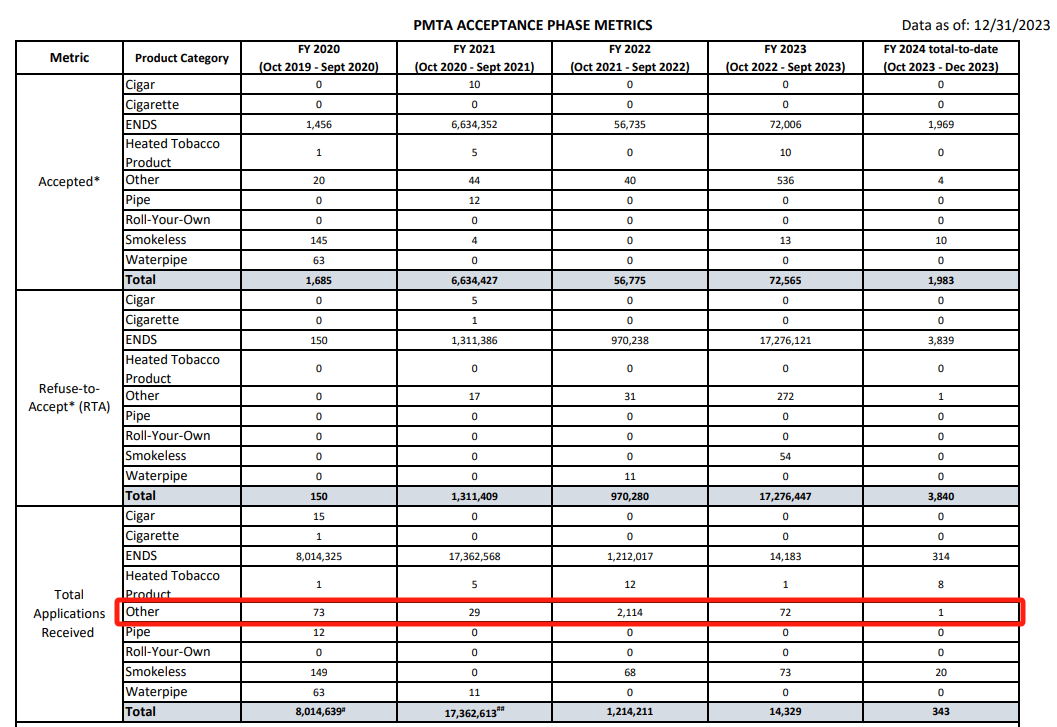
在获得受理的申请中,FDA最终仅在2021年9月19日授权由美国无烟烟草公司(U.S. Smokeless Tobacco Company LLC)以Verve品牌生产的4种新型口含烟产品上市销售。其它剩余的产品或者在审核中或者收到了FDA颁发的营销拒接令(MDO)。

这4款口含烟产品(口含片)名称分别是Verve Discs Blue Mint、Verve Discs Green Mint、Verve Chews Blue Mint 和 Verve Chews Green Mint。
这些产品成分主要特点包括:
1)使用了烟草来源的尼古丁,且均为药品级纯度;
2)尼古丁浓度在1.5mg/片;
3)口味均为薄荷味。

2)青少年、非吸烟者和前吸烟者不太可能开始或重新开始使用这些烟草产品。
此外,FDA也对Verve产品的营销方式进行严格限制,包括限制通过网站和社交媒体平台销售,以确保营销仅针对成年人。
但自从2022年4月14日发布对于含有非烟草尼古丁(NTN)的尼古丁袋需满足联邦法律H.R.2471的相关要求以来,就一直没有相关尼古丁袋(口含烟)产品获得过上市授权许可。目前对于非烟草尼古丁(NTN)产品FDA还在考虑中,可能会影响这类产品的营销授权许可。
2024年4月4日,FDA宣布向2023年10月至2024年2月期间在未成年人之间销售各种口味的ZYN尼古丁袋的实体零售商发出119封警告信,并提出41起民事罚款投诉。美国食品药品监督管理局(FDA)还向三家在线零售商发出了警告信,因为它们销售未经授权的调味ZYN尼古丁袋,包括espresso、Black Cherry、Lemon Spritz和Cucumber Lime。FDA发警告信的主要原因是ZYN品牌尼古丁袋在青少年人群当中使用比例高。目前美国青少年使用的烟草产品中,尼古丁袋占比为1.5%。
但尼古丁袋以其低毒性的特点也是被监管机构所看到的,根据两个至上引用tobacco harm reduction统计的15类型尼古丁产品的相对风险等级,尼古丁袋的使用风险甚至比电子烟及HNB等产品要更低,更不用说传统烟草产品。见下图
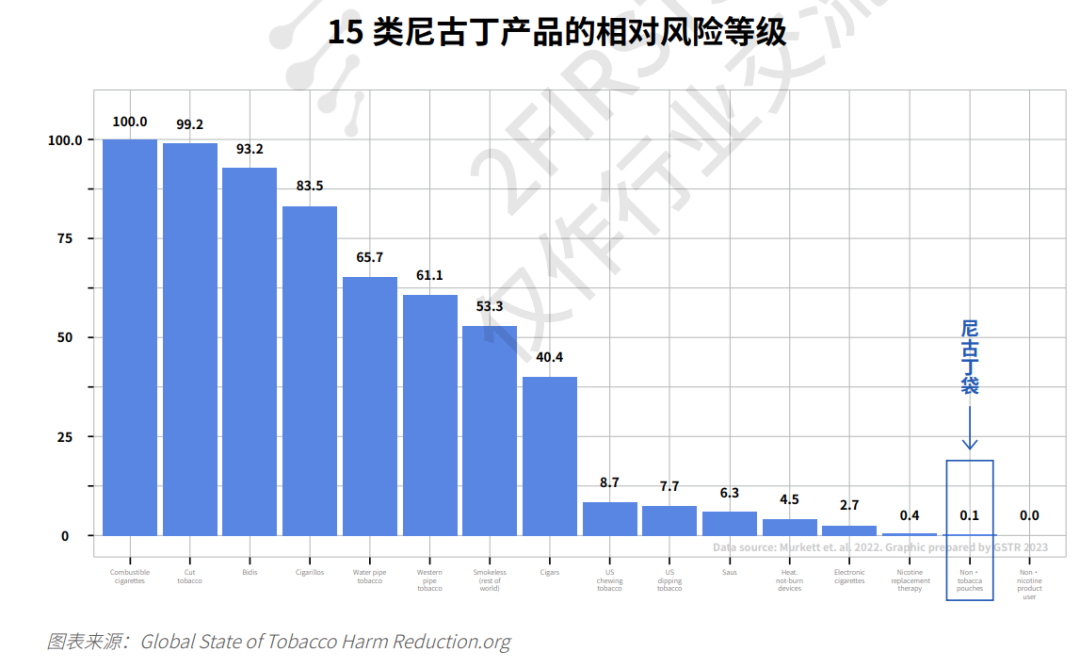
最近据新闻报道,美国前FDA局长斯科特·戈特利布(Scott Gottlieb)称ZYN尼古丁袋助美国人戒烟,呼吁优先审批低风险烟草产品。
目前英柏检测可以根据产品特点以及法规的要求为各类尼古丁袋产品申请PMTA,有需要的企业可以联系洽谈沟通。尼古丁袋是三大新型烟草之一,目前也是大烟草公司主营增长最快的产品线,美国市场也是仅次于欧盟第二大尼古丁袋市场,企业可以尽早布局,争取早日上市售卖!
若您有疑问
本文指导老师:消费品事业部 Frank